KESETIMBANGAN KIMIA
(Chapter 14.1 - 14.3)
Konsep Penting
• Kita mulai dengan membahas sifat keseimbangan dan perbedaan antara keseimbangan kimia dan fisika. Kami mendefinisikan konstanta kesetimbangan dalam hal hukum aksi massa. (14.1)• Kita kemudian belajar menulis persamaan konstanta kesetimbangan untuk kesetimbangan homogen dan heterogen. Kita melihat bagaimana mengekspresikan konstanta kesetimbangan untuk banyak kesetimbangan. (14.2)
• Selanjutnya, kita menguji hubungan antara konstanta laju dan konstanta kesetimbangan dari suatu reaksi. Latihan ini menunjukkan mengapa konstanta kesetimbangan adalah konstan dan mengapa itu bervariasi dengan suhu. (14.3)
Keterangan
- K = tetapan kesetimbangan
- [A] = molaritas zat A .................................. (M)
- [B] = molaritas zat B .................................. (M)
- [C] = molaritas zat C ...................................(M)
- [D] = molaritas zat D .................................. (M)
Tetapan kesetimbangan (K), sering juga dituliskan KC . Pada buku ini digunakan simbol KC untuk harga tetapan kesetimbangan.
Kita telah melihat bahwa K adalah konstan pada suhu tertentu terlepas dari variasi konsentrasi kesetimbangan individu. Kita dapat mencari tahu mengapa demikian dan pada saat yang sama mendapatkan pemahaman tentang proses kesetimbangan dengan mempertimbangkan kinetika reaksi kimia.
Misalkan reaksi yang dapat dibalik berikut ini terjadi melalui mekanisme yang terdiri dari satu langkah dasar baik dalam arah maju maupun mundur:
laju maju diberikan oleh
dan nilai sebaliknya diberikan oleh
dengan kf dan kr adalah konstanta laju untuk arah maju dan mundur. Pada ekuil-librium, ketika tidak ada perubahan bersih yang terjadi, kedua tingkat tersebut harus sama:
Karena kf dan kr adalah konstanta pada suhu tertentu, rasionya juga konstan, yang sama dengan konstanta kesetimbangan Kc.
Jadi Kc selalu konstan tanpa memperhatikan konsentrasi kesetimbangan spesies yang bereaksi karena selalu sama dengan kf / kr, hasil bagi dua kuantitas yang dengan sendirinya konstan pada suhu tertentu. Karena konstanta laju bergantung pada suhu [lihat Persamaan (13.11)], maka konstanta kesetimbangan juga harus berubah dengan suhu. Sekarang anggaplah reaksi yang sama memiliki mekanisme dengan lebih dari satu tahap dasar. Misalkan itu terjadi melalui mekanisme dua langkah sebagai berikut:
Ini adalah contoh beberapa kesetimbangan, Kami menulis ekspresi untuk konstanta kesetimbangan:
Mengalikan Persamaan (14.10) dengan Persamaan (14.11), kita dapatkan
Untuk reaksi keseluruhan, kita bisa tulis
Karena K' dan K" adalah konstanta, Kc juga konstanta. Hasil ini memungkinkan kita menggeneralisasi perlakuan kita terhadap reaksi
Terlepas dari apakah reaksi ini terjadi melalui mekanisme satu langkah atau multistep, kita dapat menulis ekspresi konstanta kesetimbangan menurut hukum aksi massa :
Singkatnya, kita melihat bahwa dalam istilah kinetika kimia, konstanta kesetimbangan suatu reaksi dapat dinyatakan sebagai rasio konstanta laju reaksi maju dan mundur. Analisis ini menjelaskan mengapa konstanta kesetimbangan adalah sebuah konstanta dan mengapa nilainya berubah seiring dengan suhu.
Contoh soal
Satu liter campuran gas pada suhu 100°C pada keadaan setimbang mengandung 0,0045 mol dinitrogen tetraoksida dan 0,03 mol nitrogen dioksida.
- Tuliskan rumus tetapan kesetimbangan gas tersebut.
- Hitung tetapan kesetimbangannya.
Jawab:
N204(g) ⇄ NO2(g)
Persamaan di atas harus disetarakan dulu menjadi
N204(g) ⇄ 2NO2(g)
a. Tetapan kesetimbangan dituliskan sebagai perbandingan molaritas produk (nitrogen dioksida) dengan molaritas reaktan (dinitrogen tetraoksida) yang masing-masing dipangkatkan dengan koefisiennya, sehingga dapat dituliskan sebagai berikut.


Jadi, tetapan kesetimbangannya sebesar 0,2.




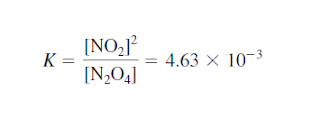



















Tidak ada komentar:
Posting Komentar